Propiedades de la materia, mezclas, características, y Leyes de la combinación Química.
Todo aquello que nos rodea a los seres humanos cambia constantemente: el hombre y mujeres, habitantes del mundo, se desplazan, se alimentan , se relacionan entre si y con la naturaleza que cobija o amenaza. La química se ocupa, precisamente, de las transformaciones que se producen en la materia y la energía, desde el estudio de los átomos y otras partículas imperceptibles a simple vista hasta el comportamiento de los grandes astros del universo. por lo tanto el presente blog contiene información acerca de la denominada materia, sus propiedades, características y mucho mas.
Química
La química es una rama de las ciencias que se encarda de estudiar la composición de la materia y los cambios que en ella ocurren o puedan ocurrir.
 |
Origen de la química
Se pueden resumir en 6 periodos
Pre histórico
· Incia 500 a.c.
· con el descubrimiento del fuego y este se implementó para la preparación de alimentos
· sin embargo 2000 años antes de cristo, los chinos ya elaboraban la seda artificial, papel, la pólvora entre otros.
· De igual manera en Egipto purificaban el oro, la plata y otros metales; pero el más resaltante era el embalsamiento de sus muertos, para la cual usaban la cera de abeja y algunos aceites y reciñas obtenidos de la naturaleza
Griego
· De 500 a.c – 300 a.c
· La química se basó en una visión filosófica
· La contribución más importante en este periodo fue dada por los filósofos Leucipo y Demócrito, quienes establecieron que la metería está formada por átomos.
· De 300 a.c – 1500 d.c
· La mejor época de este periodo fue en el año 1400 d.c
· Se basó en la búsqueda de sustancias míticas
· Gracias a esto se descubrió el antimonio y el fosforo
· Gracias a la alquimia se desarrollaron algunos de los instrumentos de laboratorio que conocemos hoy en día
Iatroqumíca
· 1500 – 1600
· Se inicia la transición de la verdadera química
· Denominada química medica
· Cuyo fin era buscar las propiedades medicinales de diferentes sustancias
· Implementando el método experimental
· 1660 – 1770
· Se mejora el método experimental por Robert Boyle
· Separación de la química de la teoría alquimista
· Objetivo principal de la química era encontrar las diferencias de las sustancias
· Se formula la teoría del flogisto
· De 1770
· Joseph Priestley aísla el oxigeno como un gas que hace arder con mayor intensidad la llama de una vela
· Antoine Lavoisier quien explica los procesos de combustión, respiración y calcinación; composición del aire identificando el oxígeno y el nitrógeno entre otros.
· John Dalton con la teoría atómica
Y muchos más que dieron aportes para lo que hoy en día se conoce en química:
· Mendeléyev creado de la tabla periódica
· JJ Thomson descubre el electrón
· Niels Bohr publica su modelo de estructura atómica
· Entre otros
La materia
Todo aquello que nos
rodea es materia: la mesa, la cama, los libros, el agua que bebemos, el aire
que respiramos. Entonces podemos definir esta, como todo aquello que ocupa un
lugar en el espacio y se puede pesar.
Propiedades de la materia
Las propiedades son
aquellas que nos permiten diferenciar la materia de cosas inmateriales, en este
caso hay dos tipos de propiedades, las propiedades generales y las especificas.
Propiedades generales
Son
características comunes a todos los cuerpos como lo son:
· Masa: cantidad de materia que contiene un cuerpo
· Volumen o extensión: espacio que ocupa un cuerpo
· Peso: la fuerza que ejerce la gravedad sobre los
cuerpos
· Porosidad: espacio que existe entre las partículas
· Inercia: característica que impide a la materia
moverse sin intervención de una fuerza externa
· Impenetrabilidad: propiedad de que un cuerpo no puede
usar el espacio de otros cuerpos al mismo tiempo
· Divisibilidad: capacidad de la materia dividirse en
partes más pequeñas
Es
importante saber que la materia y sus propiedades siempre estarán afectadas por
la fuerza gravitacional del medio en donde se encuentren y también por la
fuerza de atracción entre las moléculas que la componen
Propiedades
específicas de la materia
Son las que
diferencian un cuerpo de otro y son agrupadas.
·
Propiedades físicas: son definidas como las
estructuras que se pueden medir; sabor, textura, estado físico
·
Propiedades químicas: propiedades en la que cada
sustancia tiene un respecto y otras tienen la habilidad de crear cosas nuevas; la
oxidación, la afinidad electrónica, la reactividad ente otros.
Clasificación
de la materia
Sustancias
puras: Son aquellas que no se pueden descomponer en otras, con una composición
fija y un único conjunto de propiedades
Mezclas: Es la que está
compuesta por dos o más sustancias puras, que se manifiestan de manera
homogénea (son en las que sus componentes no se distinguen a simple vista) y
heterogenia (en las que sus componentes se pueden distinguir)
Las mezclas y sus características
principales
1.
Sus componentes se pueden separar
2.
Poseen composiciones variables
3.
Pueden tener una o más fases
4.
Pueden ser radiactivas
Métodos
de separación
Existen diferentes métodos para separar una mezcla en
sus diferentes componentes. Los métodos son físicos que no alteran las
propiedades de los componentes. A continuación,
conoceremos cuales son estos métodos:
Evaporación: Método físico
que permite separar un sólido de un líquido que se encuentra en una mezcla
homogénea.
Cristalización: Método que se
usa para separar una mezcla de un sólido en un líquido.
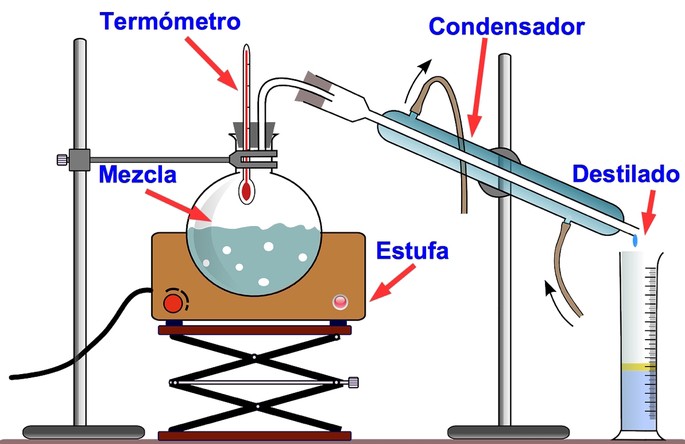
Destilación: Método que consiste
en separar dos o más líquidos miscibles con diferentes puntos de ebullición,
primero por la evaporación y luego por la condensación de las sustancias.
Filtración: Se trata de una
operación que permite separar mezclas heterogéneas de un sólido insoluble en líquido.
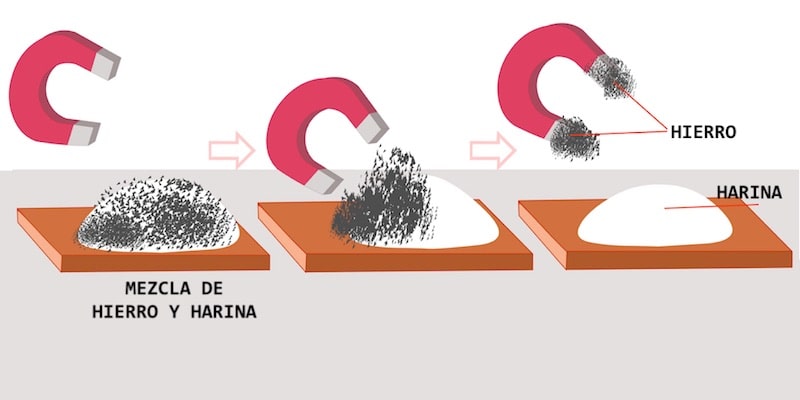
Imantación: Consiste en
separar con un imán los componentes de una mezcla de un material magnético y
otro que no lo es.
Conservación
de la materia
En cualquier reacción química la masa se conserva,
esto quiere decir, que la misma se mantiene tanto en el reactivo como en el
producto.
Proporciones definidas (ley de proporción constante)
En esta ley se establece que cuando se combinan dos o más
elementos para lograr un determinado compuesto siempre se combinara en una
proporción constante de masas.
Proporciones
múltiples (ley de proporciones múltiples de Dalton)












Comentarios
Publicar un comentario